Acidobazická rovnováha je mezi mediky takové neoblíbené téma. Ostatně není se čemu divit. Během studia se v různých předmětech probírá opakovaně, člověk ji několikrát vůbec nepochopí a následně ji po pochopení opakovaně zapomíná. Já se ji pokusím vysvětlit pokud možno jednoduše a lidsky po jednotlivých bodech.
1. Úvod
Lidské tělo potřebuje pro zdárný průběh metabolických reakcí stabilní vnitřní prostředí a stabilní vnitřní prostředí je udržováno na principu tzv. dynamické rovnováhy. To znamená, že jednotlivé parametry vnitřního prostředí se neustále mění, ale v ideálním případě jsou tyto změny pouze v určitém malém rozmezí. Mezi zmíněné parametry určující vnitřní prostředí patří řada veličin – teplota, koncentrace jednotlivých sloučenin a pak také pH. A právě pH se týká ona acidobazická rovnováha.
2. Co je to pH?
pH je fyzikální veličina, která určuje „kyselost“ vodného prostředí, tj. množství kationtů vodíku H+. Přesně řečeno je pH záporný dekadický logaritmus koncentrace H+. Naštěstí jsme nešli na medicínu, abychom se zabývali nějakými logaritmy, takže si s tím nemusíme zatěžovat naše krásné hlavičky. Nám bude stačit zapamatovat si dvě pravidla.
- Za prvé: Čím je prostředí kyselejší, tím je pH nižší.
- Za druhé: V lidském těle se pH pohybuje mezi 7,35-7,45. Větší výchylku dokážeme sice určitou dobu vydržet, ale při jejím trvání a prohlubování zpravidla umíráme.
3. Odchylky pH
Zmíněné pH našeho organizmu je vychylováno neustále. Za prvé přijímáme do organizmu sloučeniny, které mají kyselejší nebo zásaditější charakter. Za druhé – a to je mnohem podstatnější – řada sloučenin s potenciálem vychýlit pH v našem organizmu neustále vzniká v důsledku probíhajících metabolických reakcí. A vyplatí se zdůraznit, že většina těchto metabolických produktů je kyselá a má tendenci snižovat pH.
4. Pufrační systémy
Z důvodu výše uvedeného musí v našem organizmu fungovat tzv. pufrační systémy. Úkolem pufračního systému je „absorbovat“ působení každého faktoru, které by vedlo ke změně pH. Pufračních systémů máme více, ale nejvýznamnější a na vysvětlení nejvděčnější je bikarbonátový systém související s kyselinou uhličitou (H2CO3). Tato slabá kyselina ve vodném prostředí organizmu existuje ve dvou základních formách, které v sebe vzájemně přecházejí:
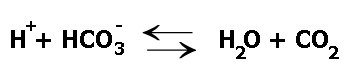
Základní rovnováha bikarbonátového pufračního systému
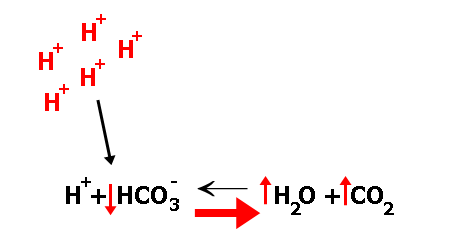
Zde vidíme reakci bikarbonátového systému na kyselé prostředí. Rovnováha se posune ve směru červené šipky, HCO3- klesá, zatímco CO2 stoupá. Ovšem to nevadí, CO2 zvládneme vydýchat.
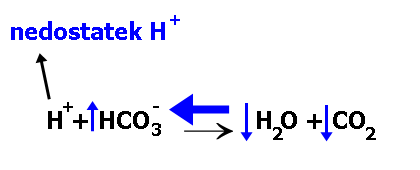
A zde vidíme reakci bikarbonátového systému na zásadité prostředí. Rovnováha je posunuta opačně ve smyslu modré šipky, koncentrace HCO3- proto roste, zatímco koncentrace CO2 klesá.
Kromě bikarbonátového existuje ještě pufrační systém hemoglobinu, fosfátů, bílkovin a amoniaku. Bikarbonátový systém má oproti nim tu zásadní výhodu, že koncentrace jedné z jeho složek (tj. CO2) je snadno regulovatelná (vydýchatelná) plícemi. Ale souvisí s tím i jedna velká nevýhoda. Při primární poruše funkce plic není bikarbonátový systém schopen narušení vnitřního prostředí kompenzovat, protože je součástí problému. Tady se musí na kompenzaci podílet ostatní pufrační systémy.
5. Kompenzační orgány
Pufry dokážou prakticky okamžitě stabilizovat odchylky, ale ke své činnosti z dlouhodobého hlediska potřebují správnou funkci některých orgánů, které se na udržení stabilního pH podílí také. Jde zejména o plíce, ledviny a játra.
Plíce fungují stran ovlivnění acidobazické rovnováhy velmi rychle a vydýcháváním CO2 „uleví“ bikarbonátovému pufračnímu systému. Nicméně si můžete povšimnout, že nevyřeší přítomnost kyselých sloučenin a vyčerpávání zásob HCO3-. Proto potřebujeme, aby se zapojily i ledviny. Kompenzace acidobazické rovnováhy ledvinami je sice relativně pomalá (plíce jsou rychlejší), ale je velice efektivní. Ledviny vylučují H+ do moči a tím přímo snižují kyselost. Kromě toho jsou ledviny dle situace schopny vylučovat do moči HCO3-, ale také ho z moči zpětně resorbovat do organizmu.
Běžně se to moc neudává, ale kromě plic a ledvin mají na udržení acidobazické rovnováhy velký podíl i játra. Jde o „chemickou továrnu“ těla, kde vzniká celá řada sloučenin a jejich vznik nebývá pH neutrální (laktát, proteiny, ketolátky, močovina apod.). Regulace syntézy těchto sloučenin se pak může podílet na udržení stabilního pH. Například přeměna amoniaku na močovinu (močovinový cyklus) vede k produkci H+ a v případě acidózy je tendence vznik močoviny tlumit.
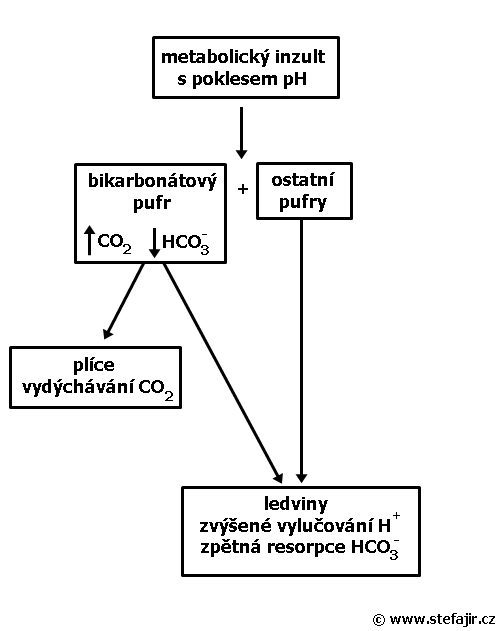
Schéma reakce na "kyselý" metabolický inzult, což je pro náš organizmus běžná zátěžová situace. Nejrychleji zareagují pufrační systémy. Na bikarbonátový systém rychle navazují plíce, které vydýchají nahromaděný CO2. Později navazují ledviny, které vylučují H+ a zpětně resorbují HCO3-. (Játra pro zjednodušení ponechávám stranou.)
Poruchy acidobazické rovnováhy
Existují celkem čtyři základní poruchy acidobazické rovnováhy – metabolická acidóza, metabolická alkalóza, respirační acidóza a respirační alkalóza. Acidóza znamená pokles pH, alkalóza jeho zvýšení. Respirační typ poruchy vzniká v důsledku nedostatečné nebo naopak zvýšené funkce respiračního systému, metabolický typ poruchy ve šech ostatních případech (např. zvýšená tvorba kyselých sloučenin v organizmu, ztráty kyselého žaludečního obsahu při zvracení, porucha funkce ledvin apod.).
U jednoho pacienta se může vyskytovat jedna z těchto poruch nebo jejich kombinace. Za zmínku stojí, že nejčastějším problémem je metabolická acidóza. Pokud jde o pH, tak po určitou dobu může zůstat ve svém normálním rozmezí nebo se jen mírně odchýlit (kompenzace) s následným výraznějším poklesem u acidózy nebo zvýšením u alkalózy (dekompenzace).
-
Metabolická acidóza – Metabolická acidóza je typickým problémem, kterému musí naše vnitřní prostředí čelit. Podstatná část produktů našeho metabolismu je kyselá a kromě toho se může organizmus dostat do kontaktu s kyselými sloučeninami ze zevního prostředí, nebo je narušena schopnost ledvin kyselé sloučeniny vylučovat. Více najdete v textu o acidóze.
-
Metabolická alkalóza – Je méně častá než metabolická acidóza a vzniknout může v důsledku opakovaného úporného zvracení se ztrátou kyselého žaludečního obsahu, který se tělo snaží doplňovat. Více najdete v textu o alkalóze.
-
Respirační acidóza – Vzniká v důsledku hromadění CO2 při respirační nedostatečnosti u nejrůznějších plicních onemocnění. Více najdete v textu o acidóze.
-
Respirační alkalóza – Může se objevit při velmi usilovné hyperventilaci, která vede k poklesu koncentrace CO2. Více najdete v textu o alkalóze.
Diagnostika
Pokud pomineme klinický stav pacienta, acidobazickou rovnováhu a její poruchy můžeme diagnostikovat z několika parametrů. Ideálním zdrojem je vzorek arteriální krve (běžně odebíraná z arteria radialis) a v něm zjišťujeme pH, pO2, pCO2, koncentraci HCO3- a base excess (BE). Toto vyšetření označujeme jako Astrup (detaily viz příslušný text).
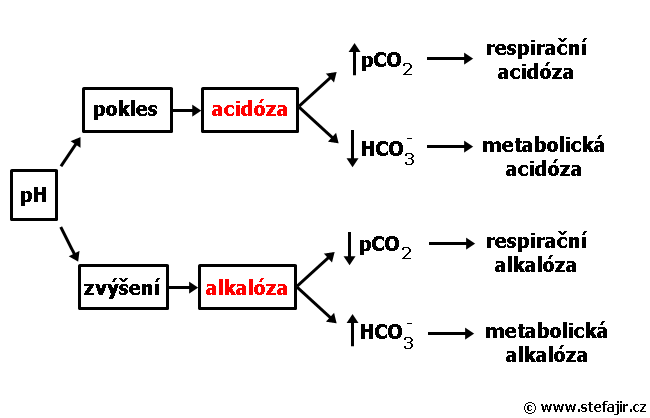
Zjednodušené schéma ukazuje interpretaci těch hlavních hodnot Astrupu. Se znalostí pH, koncentrace CO2 a HCO3- se dají určit méně komplikované formy poruch acidobazické rovnováhy.
Proč je to důležité?
-
Kussmaulovo dýchání je typickou kompenzační odpovědí plic na metabolickou acidózu a můžeme ho najít u těžce dekompenzovaných diabetiků 1. typu. Jde o rychlé a hluboké dýchání, které umožňuje odstraňovat CO2 z krve. Více najdete v příslušném textu.
-
Terapeutické řešení metabolické acidózy je různé podle její tíže a vyvolávající příčiny. Pokud je lehčího rázu, mnohdy postačí léčit vyvolávající příčinu a nechat organizmus, aby situaci normalizoval vlastními regulačními mechanizmy (například zaléčit dekompenzovanou cukrovku 1. typu), u těžších forem s poklesem pH lze podávat bikarbonát, který zvyšuje zásaditost prostředí. Pokud pH klesne k 7,1 a níže, může již být zvažována dialýza, která dokáže vnitřní prostředí upravit velmi účinně.
-
Těžká metabolická acidóza vzniklá požitím nějaké sloučeniny je typická pro otravu metanolem a otravu etylenglykolem.



